Nature子刊:胡全银团队开发基于血小板的靶向蛋白降解技术——DePLT
来源:生物世界 2024-12-09 09:54
该研究开发的基于血小板的靶向蛋白降解(TPD)策略,克服了常用嵌合体的局限性,有助于推进TPD技术的体内治疗应用。
威斯康星大学麦迪逊分校胡全银团队在 Nature Biotechnology 期刊发表了题为:Engineered platelets as targeted protein degraders and application to breast cancer models 的研究论文。
该研究开发了基于血小板的靶向蛋白降解技术——DePLT,并将其应用于乳腺癌治疗。


胡全银于2018年获得北卡罗来纳大学教堂山分校和北卡罗莱纳州立大学的生物医学工程博士学位,导师为顾臻教授(现为浙江大学药学院院长);2018-2020年在麻省理工学院Robert Langer教授实验室从事博士后研究工作,此后于2020年加入威斯康星大学麦迪逊分校,任药学院助理教授。
尽管前景广阔,靶向蛋白降解(TPD)技术使用的嵌合体分子独特药理学面临着一些固有挑战,尤其是在体内应用时。在结构上,嵌合体分子通常具有不良的类药物特性,可能表现出在靶部位的蓄积不足,并且与两种不同的生物活性配体相关的脱靶或组织外的靶副作用风险增加。在机制上,泛素-蛋白酶体系统(UPS)和溶酶体介导的TPD都需要形成嵌合体-效应体-目标蛋白的三元复合物,这需要局部嵌合体剂量和两种蛋白丰度之间的精确时空协调,这为嵌合体的开发带来了与传统疗法(例如小分子和抗体药物)相比的额外挑战。
为了解决上述挑战,研究团队开发了一种基于血小板的靶向蛋白降解方法,将目标蛋白的配体与血小板内的HSP90(热休克蛋白90)通过NASA连接子共价连接,从而构建出降解剂血小板(Degrader Platelet,DePLT),其可选择性地聚集在出血部位,并通过重新利用HSP90在蛋白质加工中的作用,有效地降解目标蛋白。基于不同的目标蛋白配体和HSP90转运机制,活化的DePLT分别通过泛素-蛋白酶体系统(UPS)或溶酶体介导的机制实现对细胞内或细胞外的蛋白质的降解清除。
预先标记的HSP90被包装到血小板来源的微粒(PMP),通过膜融合进入靶细胞,并利用UPS降解细胞内的目标蛋白,而与配体拴系在一起的游离HSP90则重定向细胞外靶点,使其被溶酶体降解。
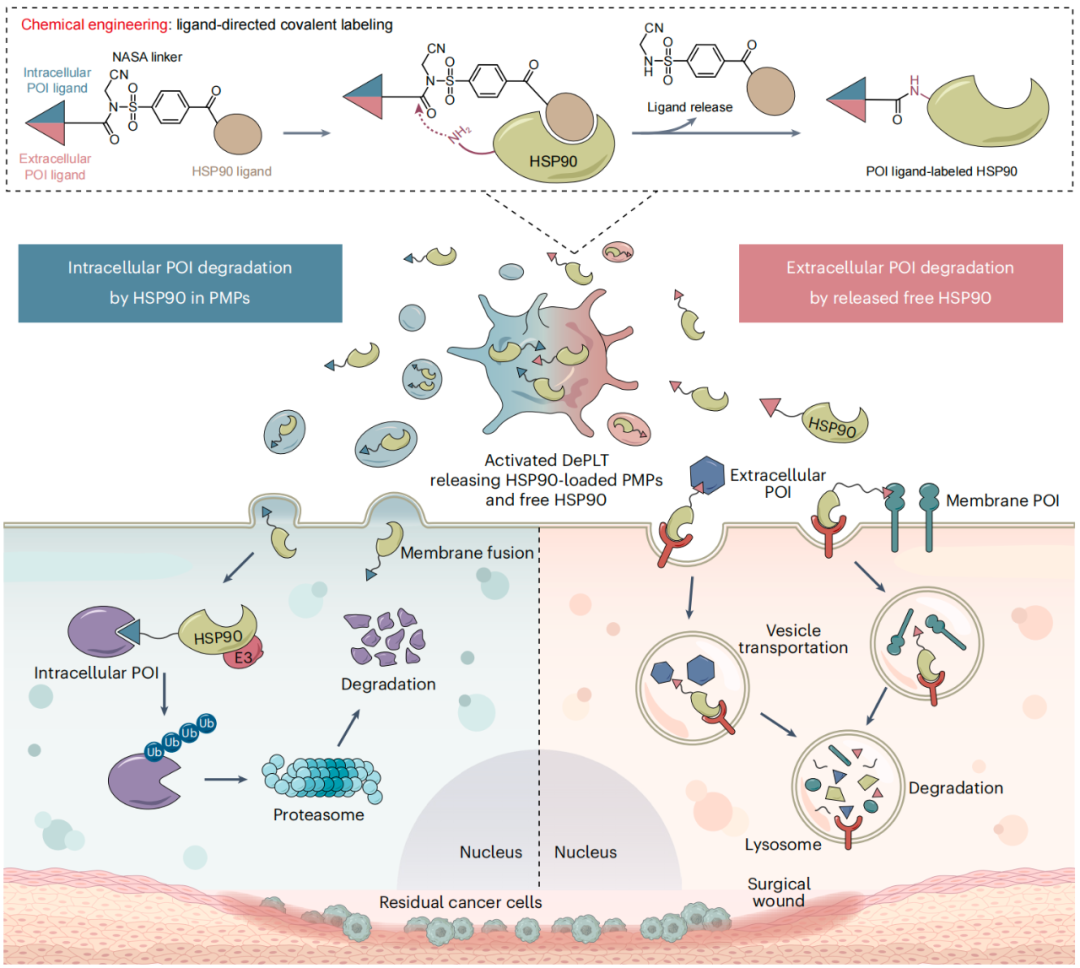
研究团队进一步证明,三阴性乳腺癌(TNBC)小鼠术后模型中,DePLT能够靶向降解细胞内蛋白BRD4,从而抑制肿瘤的复发和转移,还能够靶向降解细胞外蛋白PD-L1,从而增强抗肿瘤免疫效果,提高生存率。
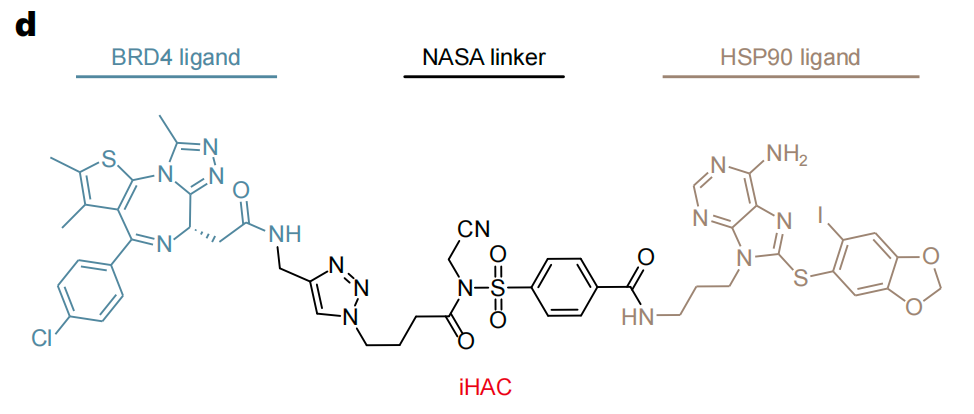
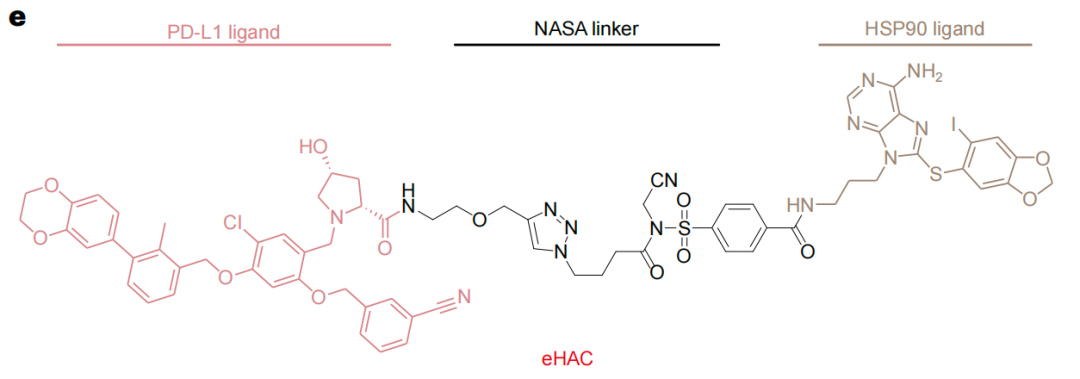
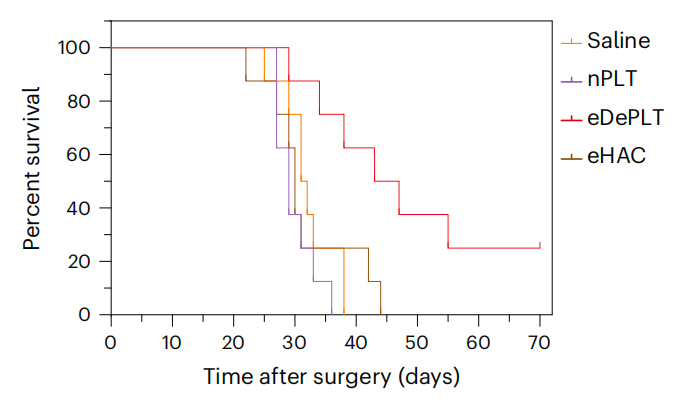
总的来说,该研究开发的基于血小板的靶向蛋白降解(TPD)策略,克服了常用嵌合体的局限性,有助于推进TPD技术的体内治疗应用。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


